下垂体炎/下垂体機能低下症 hypophysitis/hypopituitarism
下垂体炎とその疫学
・下垂体炎(hypophysitis)は自己免疫疾患、浸潤性疾患、感染性疾患、腫瘍性疾患などにより下垂体または漏斗部を局在とする炎症性疾患である。
・年間発症率は不明であるが、ある報告では900万人に1人程度と推定されている。
・炎症が視床下部まで広がることもあれば、孤発性視床下部炎(isolated hypothalamitis)として発症することもある。
分類と病因
・下垂体炎は病因により原発性と二次性とに区別される。
・原発性下垂体炎は孤発性の疾患であり、自己免疫性(例: リンパ球性下垂体炎)や特発性も含む。
・二次性下垂体炎は局所的な問題に続発して生じる疾患(例: ラトケ嚢胞の破裂)、全身性疾患、感染症、腫瘍性疾患、薬剤性に生じるものを指す。
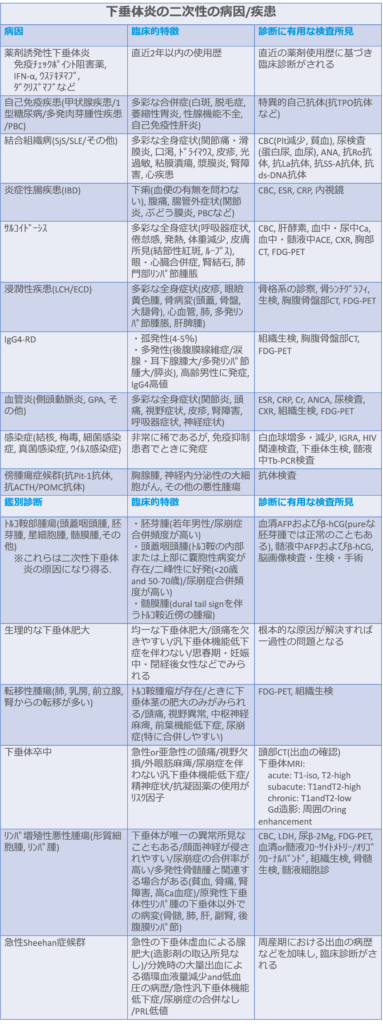
<二次性下垂体炎の病因と鑑別疾患>
臨床経過/臨床症状
・典型的には下垂体炎では肥大した下垂体および漏斗部(下垂体茎)による圧迫(mass effect)に起因する頭痛と視野変化を呈する。
・患者の約半数で頭痛を自覚し、10~30%でmass effectによる視野障害を自覚する。
・前葉and/or後葉のホルモン欠乏症に起因する症状はその原因と傷害の程度により異なる。
・一般的には前葉機能不全と尿崩症の両者が併存する場合には炎症性疾患、浸潤性疾患、頭蓋咽頭腫、または転移性腫瘍の可能性が考えやすい。一方で、下垂体腺腫の可能性は低い。
・リンパ球性下垂体炎(LHy)および免疫療法による下垂体炎では炎症により主にACTHに影響を及ぼしやすく、それに次いでゴナドトロピン、TRHに影響を及ぼしやすい。下垂体腺腫ではACTHが最も影響を受けにくい(影響を受けるのが終盤)という典型像と異なるという点が重要である。
・下垂体炎を疑う全ての患者は各種生化学検査を要する。午前08時時点でのコルチゾール(and/or ACTH刺激試験)、TSH、FT4、PRL、LH、エストラジオール(E2)、テストステロン、FSH、IGF-1を測定し、尿崩症の存在が疑われる場合には血清ナトリウム、血漿浸透圧、尿浸透圧などを測定する。
・副腎不全、重度の甲状腺機能低下症、SIADでは低ナトリウム血症が、代償不全の尿崩症では高ナトリウム血症が認められることがある。
下垂体炎の画像上の特徴
・下垂体炎では様々な画像所見がみられる。
・下垂体炎で最もよくみられるMRI所見は偏倚がなく肥厚した下垂体茎(a thickened nondeviated stalk)であり、患者の80%以上でmild-moderateの下垂体の対称性腫大を伴う。なお、下垂体腺腫では下垂体茎に偏倚を伴う点が異なる。
・下垂体炎では造影剤の取込み所見が通常、均一的であり、不均一であることは少ない。
・下垂体腺腫ではトルコ鞍底部(sellar floor)が侵されやすいが、下垂体炎では侵されにくい。
・下垂体炎では後葉における炎症によりADH顆粒の減少が生じ、後葉のBright spotが消失しやすい。通常は後葉がT1WIで高信号を示すが、(Bright spotと呼ぶ)、下垂体炎ではこの所見が消失する。
・硬膜におけるDural tail signが認められることもある。なお、この所見は髄膜腫でも見られることがある。
・臨床後期においては下垂体が萎縮してみえることがある(empty sella)。
生検
・生検により下垂体炎の組織学的診断が確定し、腫瘍などの病因が除外される。
・しかし、生検は侵襲性が高く、リスクとメリットとを慎重に考量しなければならない。
・生検は通常、初期検査後に診断が不明確な場合や、治療(例: 長期のステロイド, 免疫抑制, 化学療法)を行ううえで病理結果が重要なケースなどで考慮される。
・成人患者でコンセンサスが得られた生検の適応基準は存在しない。
検討される検査
・前述のように下垂体炎が疑われる場合にはまず初期検査として、午前08時時点でのコルチゾール(and/or ACTH刺激試験)、TSH、FT4、PRL、LH、エストラジオール(E2)、テストステロン、FSH、IGF-1を測定し、尿崩症の存在が疑われる場合には血清ナトリウム、血漿浸透圧、尿浸透圧などを測定する。
・下垂体生検は唯一、確定診断を可能にする検査であるが、侵襲性が高いため、慎重に考えなければならない。
・検査を検討するうえで重要なのは疫学的情報である。
・たとえば若年女性における下垂体茎肥厚はリンパ球性下垂体炎(LHy)を示唆するが、小児や思春期の患者では胚芽腫を想定した検査を実施しなければならない。高齢者ではリンパ腫をはじめとした悪性疾患を考慮することとなる。
・基本的な検査としては血液検査ではCBC、ESR、CRP、Ca、Crなどのほか、尿検査が実施される。ほかにIgG4、ACE、ANCA、ANA、LDH、β-2MG、AFP、β-hCG、IGRAなどが検討される。
・抗下垂体抗体が存在することはあるが、この抗体は下垂体腺腫だけでなく、下垂体が関与しない他の自己免疫疾患のケースでも認められることがあり、特異性に欠けることに留意する必要がある。したがって、測定は臨床的意義が乏しいと考えられている。
・リンパ球性下垂体炎では抗Pit-1抗体が認められることがある。
・全身性疾患(例: サルコイドーシス、結核、多発血管炎性肉芽腫症、悪性腫瘍、IgG4-RDなど)における他の罹患部位を特定するためには全身CT撮像、FDG-PETは有効であり、組織生検を検討するべき部位を特定できる場合がある。
・孤発性の下垂体茎病変が認められ、かつリンパ球性下垂体炎を疑う状況にない患者、あるいは悪性腫瘍や浸潤性疾患が強く疑われる患者では全身の画像検査が推奨される。
・また初期検査が陰性で腫瘍性疾患や感染性疾患が疑われるケース、または進行性のホルモン機能障害、下垂体/下垂体茎病変の増大、または視力低下が進行するケースでは細胞診、フローサイトメトリー、ACE、AFP、β-hCG、培養を目的にした髄液検査が有用なことがある。
・これらの検査が全て陰性であった場合、浸潤性疾患や炎症性疾患の多くで同様の治療(全身ステロイド投与 and/or 免疫抑制療法)が適用されるため、経験的治療としてステロイド全身投与を検討することができる。
・ただし、臨床経過が芳しくないケースや、生検による確定診断が治療法選択のうえで重要なケースでは生検が検討される。
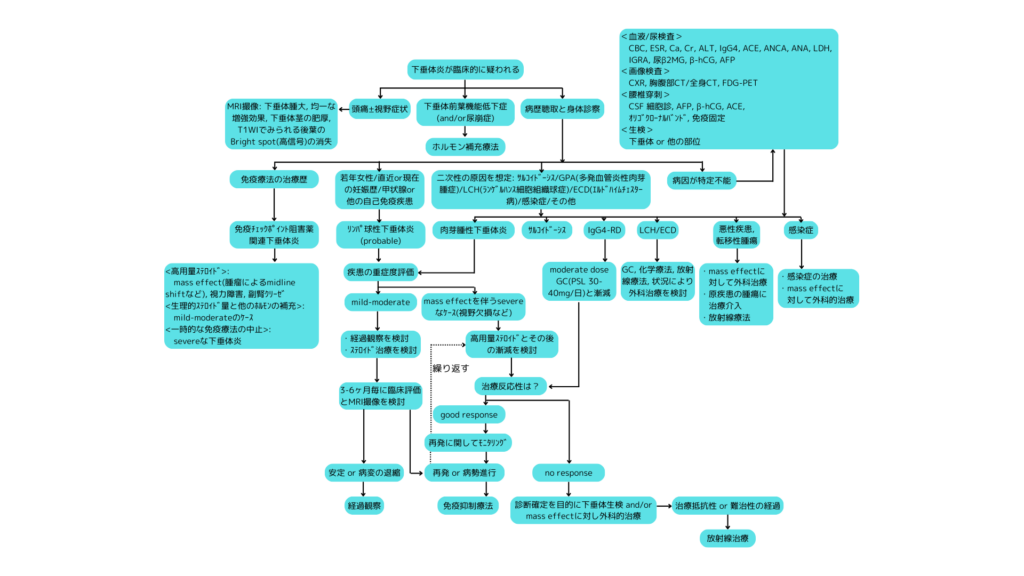
<下垂体炎の診療フロー>
治療
・下垂体炎の治療は原因疾患と重症度に応じて選択される。
・原発性下垂体炎の治療におけるPSLの用量は初期用量20mg/dayからmPSLによるパルス療法まで幅広く選択される。
・再発および治療失敗に関して、治療期間と初期投与量の間に相関性がなかったという報告もある。
<リンパ球性下垂体炎(LHy)>
・リンパ球性下垂体炎は原発性下垂体炎の約2/3を占め、女性に好発する。ただし、小児や高齢者での発症例も存在する。
・女性では妊娠中または産後早期に発症する患者が半数以上である。なお、妊娠第3期に発症のピークがある。ただし、発症と妊娠との関連性はかなり弱いと報告する研究もある。
・自己免疫疾患(例: 自己免疫性甲状腺疾患, SLE, PBCなど)の既往歴や家族歴との関連性は強く、特定の遺伝子異常も素因となることが知られている。
・重度の頭痛およびmass effectによる影響がみられるケースでは高用量ステロイド治療が第一選択となる。治療反応性は通常良好であるが、IgG4-RDのそれよりは劣る。
・なお、中枢神経リンパ腫でもステロイド治療に反応性がみられるため、治療反応性を有することは必ずしもリンパ球性下垂体炎であることを支持しない。
<肉芽腫性下垂体炎>
・肉芽腫性下垂体炎は原発性下垂体炎の約20%を占め、リンパ球性下垂体炎と同様に女性に好発し、自己免疫疾患を併発することがある。
・通常は40代で発症しやすい。
・臨床症状はリンパ球性下垂体炎と類似していて、区別が困難なこともあるが、頭痛、前葉機能低下症の頻度がより高い。また、尿崩症の合併率が高い(最大75%)。
・ステロイド治療に対する反応性はリンパ球性下垂体炎に劣る。
・また全身性疾患に関連する肉芽腫性下垂体炎では必ずしも多臓器障害を有するとは限らない点に注意する。サルコイドーシスは非乾酪性肉芽腫を形成する全身性疾患であるが、下垂体に影響を及ぼすのはサルコイドーシス症例の1%未満である。下垂体病変を有するケースでは全身性合併症を併発するリスクが高い可能性があり、71%で肺病変、58%で神経病変、38%で副鼻腔病変、33%で眼病変がみられるという報告もある。サルコイドーシスによる下垂体炎では性腺機能低下症を合併しやすく、約半数で尿崩症を合併する。
・多発血管炎性肉芽腫症による下垂体炎は稀(1%未満)であり、通常は他臓器病変も合併する。
・下垂体結核は結核の稀な合併症である。他臓器が侵されることなく、下垂体のみが侵されるケースの報告もある。典型的には発熱のない患者で、頭痛、視野障害、尿崩症を伴う汎下垂体機能低下症がみられる。生検では乾酪性肉芽腫が認められる。また、髄液中の結核菌に関するPCR検査で診断が確定できる。
<組織球症>
・組織球症のなかにはランゲルハンス細胞組織球症(LCH)、エルドハイム・チェスター病(ECD)が含まれる。
・視床下部および下垂体病変にはECDよりもLCHの方が多い。
・通常は尿崩症を合併しやすい。そのほかGH分泌異常が高率に合併する(15~50%)。
・治療法として手術、ステロイド、免疫抑制薬、化学療法、放射線療法、BRAF阻害薬、MEK阻害薬などが挙げられる。
<IgG4関連下垂体炎>
・IgG4関連下垂体炎はリンパ球およびIgG4陽性細胞の浸潤を特徴とし、進行すると花筵錠の線維化を生じる。
・比較的合併頻度が高い症状/所見としては後腹膜線維症、硬化性唾液腺炎、リンパ節腫大、膵炎などが挙げられる。そのほか間質性肺炎、腎炎なども生じ得る。
・特発性下垂体炎52例を対象としたReviewではそのなかの30~40%がIgG4関連疾患であることが後から確認された。
・診断時の平均年齢は55~65歳程度で、男性の方が多臓器に浸潤を伴うことが多い。
・IgG4関連疾患のうち、下垂体病変を伴うのは全体の4~5%とされる。下垂体のみが侵されるケースもあり、そういったケースは女性に多い傾向が示唆されている。
・全体でみれば多臓器病変を伴う頻度が高いため、全身の画像検査の実施が推奨される。PET-CTも有用である。
・MRI撮像では半数以上のケースで下垂体および下垂体茎の肥大がみられる。
・患者の15~25%では血清IgG4血が基準値内であり、その多くが女性患者である。
・治療としてはPSL 30~40mg/dayを1~2ヶ月間投与し、その後に2~6ヶ月かけて漸減する。なお、再発は稀である。
<免疫療法関連下垂体炎>
・特にCTLA-4阻害薬、PD-1およびPD-L1阻害薬の使用に関連して発症することが知られている。
・MRI撮像では画像所見が目立たないケースもあり、他の下垂体機能低下症の原因となる疾患を除外することが重要である。
・免疫療法を終了後6~15ヶ月遅れて発症するケースも報告されている。
<自己免疫性下垂体疾患>
・Paraneoplastic pituitary autoimmunityという概念があり、下垂体を標的とする自己免疫機序で下垂体疾患が発症することが明らかとなっている。
・抗体として、抗Pit-1抗体、抗ACTH抗体が知られている。
・Pit-1は下垂体前葉の細胞分化に関連する因子であるため、抗Pit-1抗体症候群ではGH、PRL、TSHの欠損をきたす。
・抗ACTH抗体を産生する腫瘍があると、それに引き続きACTH欠損が生じることがある。
・なお、Pit-1下垂体炎(Pit-1 hypophysitis)は胸腺腫、リンパ腫、胃癌、ACTH産生大細胞腫瘍などの患者でも確認されることがある。
・臨床症状はホルモン欠乏に伴う症状が主であり、頭痛は伴わない。
・画像検査では異常所見が認められないか、あっても軽度の下垂体萎縮、不均一な造影増強効果がみられるのみである。
・下垂体機能低下症は不可逆的であり、治療は原因となった腫瘍の治療とホルモン補充療法が基本となる。
――――――――――――――――――――――――――――――
<参考文献>
・Langlois F, Varlamov EV, Fleseriu M. Hypophysitis, the Growing Spectrum of a Rare Pituitary Disease. J Clin Endocrinol Metab. 2022 Jan 1;107(1):10-28. doi: 10.1210/clinem/dgab672. PMID: 34528683; PMCID: PMC8684465.